Podchlazená kapalina
Pokus číslo: 1674
Cíl pokusu
Cílem experimentu je proměřit teplotní závislost při tuhnutí kapalného pentahydrátu thiosíranu sodného a demonstrovat tak existenci podchlazené kapaliny.
Teorie
Podchlazená kapalina je kapalina, která existuje v kapalném skupenství i při teplotě nižší než je její teplota tuhnutí (odtud přímo plyne, že tento jev nemohou vykazovat amorfní látky, které přesnou teplotu tuhnutí nemají). Tento stav je metastabilní a při působení rušivých podnětů (otřesy, nečistoty) se zvyšuje pravděpodobnost, že látka spontánně přejde do stabilnějšího stavu, tj. zkrystalizuje do pevného skupenství. Při tomto přechodu se pak uvolní skupenské teplo, které látku ohřeje na její teplotu tuhnutí.
U většiny kapalin je běžně dosahované podchlazení nevýrazné, nicméně např. kapičky vody vyskytující se v mracích (cumulech či cumolonimbech) existují v kapalném skupenství i při teplotách několik desítek stupňů Celsia pod bodem mrazu. Podchlazené dešťové kapky pak v kombinaci s prochlazeným zemským povrchem vytvářejí v zimním období podmínky pro vznik ledovky.
Pomůcky
Pentahydrát thiosíranu sodného, laboratorní váhy, laboratorní stojan s držáky, tyčinka, kahan, trojnožka se síťkou, dvě kádinky různých velikostí (cca 50 ml a 200 ml), teplotní čidlo spolupracující s počítačem (ve vzorovém experimentu bylo použito čidlo Vernier Go!Temp).
Postup
Připojíme teplotní čidlo k počítači a nastavíme délku měření na půl hodiny.
Odvážíme přibližně 20 g thiosíranu a nasypeme jej do menší kádinky. Větší kádinku naplníme vodou, která bude představovat vodní lázeň.
Uspořádáme měření podle obr. 1. Do menší kádinky je zavedeno teplotní čidlo tak, aby jeho měřící prvek (špička) zůstal i po roztátí pentahydrátu ponořený. Přitom je menší kádinka s pentahydrátem zčásti ponořena do vodní lázně.
Zapneme kahan a začneme vodní lázeň zahřívat. Pokračujeme, dokud veškerý pevný pentahydrát neroztaje; teprve poté kahan vypneme.
Po vypnutí kahanu bude ještě vodní lázeň thiosíran po nějakou dobu zahřívat, jeho teplota typicky vystoupá nad 60 °C. Měření proto spustíme teprve tehdy, když teplota klesne na 55 °C. Poté měříme po celou dobu tuhnutí.
Vzorový výsledek
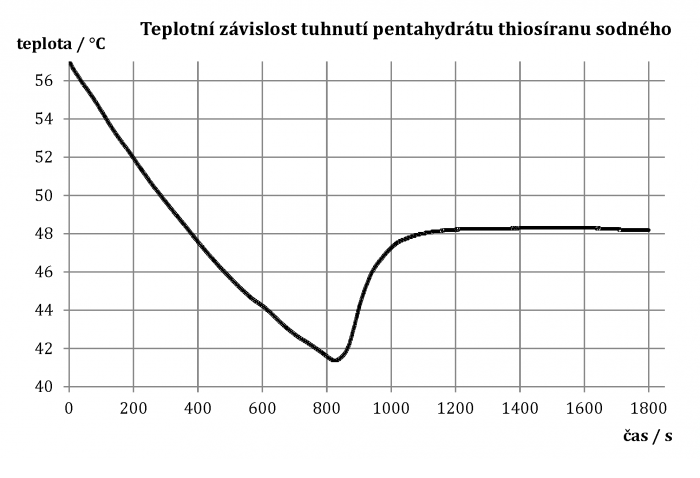
Ukázku naměřené závislosti zachycuje graf na obr. 2.
Běžně udávaná teplota tuhnutí pentahydrátu je mezi 45 °C a 50 °C. Z naměřené křivky je patrné, že jeho teplota postupně klesla pod tuto mez, přestože pentahydrát zůstával stále kapalný – stal se tzv. podchlazenou kapalinou. Přibližně při teplotě 41,5 °C pak došlo k obratu a látka se začala bez působení vnějšího zdroje zahřívat – to značí, že v tom okamžiku začala tuhnout, tedy odevzdávat skupenské teplo tuhnutí. Teplota takto stoupla až na teplotu tuhnutí, kapalina přitom zkrystalizovala; tvorba krystalků je přitom okem patrná a je zachycena na obr. 3.
Technické poznámky
Dosažená hloubka podchlazení thiosíranu velice závisí na jeho čistotě a také na čistotě kádinky, event. samotného teplotního čidla. Libovolné nečistoty mohou sloužit jako krystalizační jádra a vliv podchlazení tak výrazně snížit. Pravdou ale je, že pro pentahydrát thiosíranu sodného je tento jev tak silný, že měřitelné podchlazení zaznamenáme i za ne zcela ideálních podmínek.
Klesá-li teplota pod 30 °C a látka stále nejeví známky tuhnutí, je vhodné přibližně 5 minut před nastaveným koncem měření tuhnutí uměle iniciovat vhozením krystalků pevného thiosíranu. V opačném případě by čas nastavený na vodorovné ose nemusel stačit k tomu, abychom tuhnutí vůbec zaznamenali.
Po skončení měření zůstává v malé kádince ztuhlý pevný thiosíran. Vzhledem k jeho poměrně nízké teplotě tuhnutí stačí takovou zkumavku vymýt horkou vodou z kohoutku. Stejně tak lze kádinku znovu zahřát nad plamenem, nicméně jednou použitý thiosíran se již pro další měření ukázal jako bezcenný – ani při vyšších teplotách z něj po roztavení nevymizela pevná „vlákna“, představující výrazné nehomogenity.
Metodické poznámky
Jak je patrné ze vzorového grafu, celý sledovaný děj může trvat poměrně dlouhou dobu, třeba i 30 minut; k tomu je navíc potřeba připočítat úvodní čas nutný k roztavení pentahydrátu. Je tak vhodné tímto experimentem vyučovací hodinu začínat, aby bylo reálné jej během ní dokončit.
Během chladnutí pentahydrátu není třeba se experimentu věnovat, může probíhat na pozadí výuky. Na konci hodiny by nám ale mělo zbýt několik minut na okomentování naměřeného grafu.
Pro zajímavost lze ve výuce zmínit, že jiná pochlazená kapalina – trihydrát octanu sodného – se využívá coby náplň hřejivých polštářků (obr. 4). Tato látka zůstává při pokojové teplotě kapalná, ačkoliv její teplota tuhnutí je 58 °C. Krystalizace trihydrátu, která vede k jeho ohřátí na teplotu tuhnutí, je iniciována promáčknutím plíšku, který je do polštářků zataven.